

GMPの歴史は失敗と反省の歴史といえます(表1-1)。1937年 米国でジエチレングリコールを含んだ化学療法剤(スルファニルアミド)で107人の子供が死亡するという事件が発生し、「製造販売規制法」が制定されました。1962年のサリドマイド事件では米国は規制法があったおかげで被害をまぬがれたとも言われています。1963年にはcGMPが制定され、それ以降WHOやヨーロッパで相次いでGMPが制定されました。
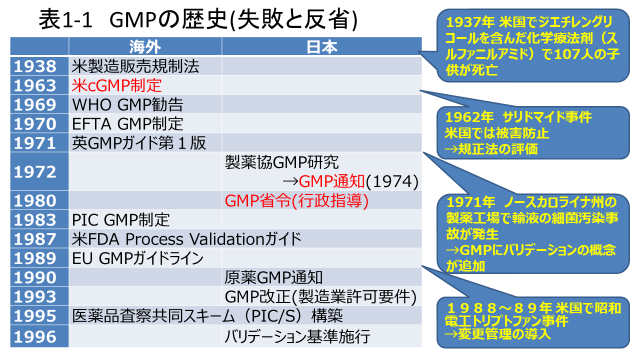
日本においても1974年にGMP通知が出され、1980年に省令化されました。
一方、1971年にノースカロライナ州の製薬工場で輸液の細菌汚染事故が発生したことをうけて。GMPにバリデーションの概念が追加されました。そして更に1988年から89年にかけて、米国で昭和電工トリプトファン事件が発生し、昭和電工が製造したトリプトファンを服用したことで、38人の死者も含む、何千人もの被害者をだしました。製造効率を高めるために、製法を変えたところ予期しない不純物が生成したことが原因と言われています。これを発端として、GMPに変更管理の考え方が導入されました。
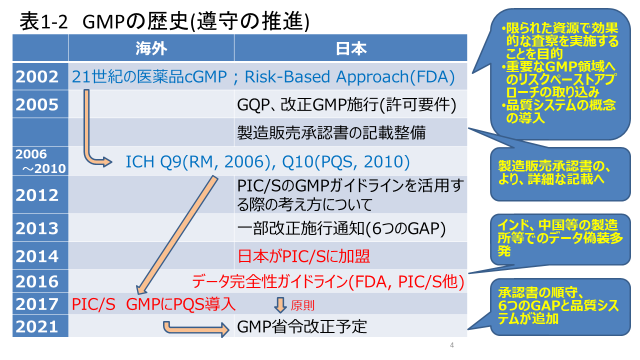
表1-2には2000年以降の流れを示しました。2000年以降は、いかにGMPを順守するか、そのための仕組みづくりが進展しました。限られた資源でGMPを適切に順守するか、それは順守する製薬企業も、それを取り締まる規制当局も同じでした。それを解決する考え方として、米国FDAから、リスクベースドアプローチの考え方と、ISO 9001をベースとした品質システムの概念が提唱されました。これがICH(日米欧三極の医薬品規制調和国際会議(当時))で取り上げられ、検討の結果、ICH Q9の品質リスクマネジメントガイドラインとICH Q10の医薬品品質システムガイドラインが発表されて、各国のGMPに取り込まれていきました。
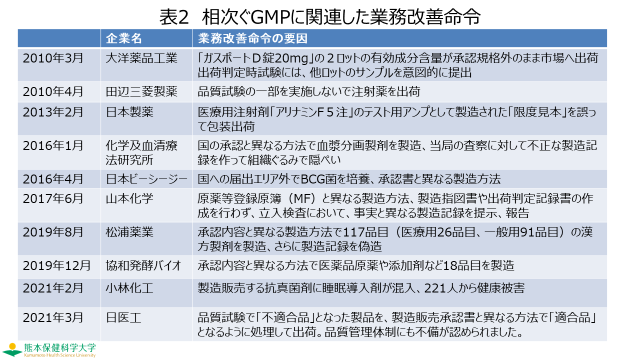
表2は、最近10年に発生したGMPに関する品質問題をまとめたものです。故意による不正が大部分ではありますが、GMP上の基本的なミスもあります。さきほどご説明したように医薬品の品質保証はサイエンスベース、リスクベースで発展し、品質システムによるGMPの遵守システムが構築されつつあるにもかかわらず、相変わらずこのような事案が発生しているということは、まだまだGMPには改善の余地があることが示唆されていると考えることが出来ると思います。
先ほど、紹介した事例の原因をそれぞれ調べていくと、「人が足りない」、「多忙だった」、「上司の指示」、「知らなかった」等のキーワードが浮かんできました。また日ごろの生産活動の中ではよく「なんでやらなければならないの」「これ、どうすればいいの」などの言葉をよく耳にします(図-3)。
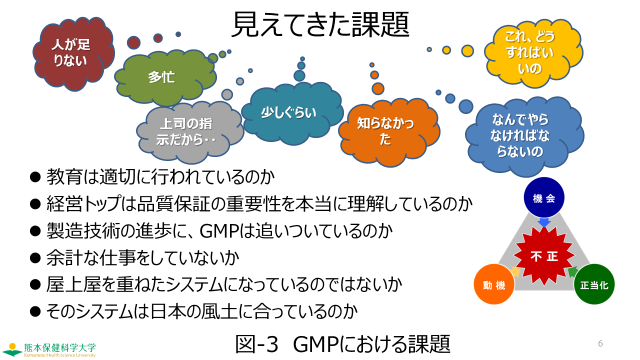
これらのことから、現在のGMPにおいて
●教育・訓練は適切に実施されているのか、
●経営トップは品質保証の重要性を理解しているのか
●製造技術の進歩に、GMPは追いついているのか
●余計な仕事をしていないか
●屋上屋を重ねたシステムになっていないか
日本の風土に合ってくるのではないかと思います
これらの課題はGMPだけの問題ではないと思います。ISO 15189の運用においても同様の課題があるのではないでしょうか。これらの課題を解決するため、当講座で現在計画しているアプローチの方法について図-4に示しました。
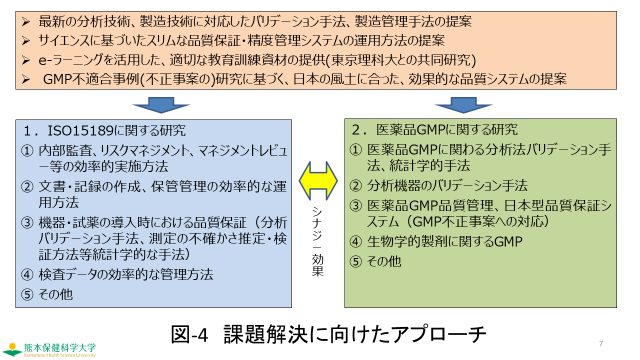
●最新の分析技術、製造技術に対応したバリデーション手法、製造管理手法の提案
●サイエンスに基づいたスリムな品質保証・精度管理システムの運用方法の提案
●e-ラーニングを活用した、適切な教育訓練資材の提供(東京理科大との共同研究)
●GMP不適合事例(不正事案の)研究に基づく、日本の風土に合った、効果的な品質システムの提案
をアウトプットとできるような研究を進めていきたいと考えています。
具体的には、ISO15189に関する分野においては
①内部監査、リスクマネジメント、マネジメントレビュー等の効率的実施方法
②文書・記録の作成、保管管理の効率的な運用方法
③機器・試薬の導入時における品質保証(分析バリデーション手法、測定の不確かさ推定・検証方法等統計学的な手法)
④検査データの効率的な管理方法
医薬品GMPに関する分野においては
①医薬品GMPに関わる分析法バリデーション手法、統計学的手法
②分析機器のバリデーション手法
③医薬品GMP品質管理、日本型品質保証システム(GMP不正事案への対応)
④生物学的製剤に関するGMP
等をテーマとして取り組んでまいります。
GMPやISO15189は実学でもあり、サイエンスでもあります。これまでも企業や規制当局中心に、実学とサイエンスがバランスしながら発展してきたものと考えます。
熊本保健科学大学にこのような講座を開設していただいたからには、私たちはサイエンスの側面からGMPの発展に貢献していきたいと思っています。
何卒よろしくお願い申し上げます。